Hersentumoren
Hersentumoren
Jaarlijks wordt in Nederland bij 100 op de 100.000 volwassenen de diagnose hersentumor gesteld. Dit is net zo vaak als bijvoorbeeld de diagnose multiple sclerose. Op volwassen leeftijd vormt de diagnose hersentumor maar een klein onderdeel van alle volwassenen die de diagnose kanker krijgen. Op kinderleeftijd komen hersentumoren minder vaak voor dan op volwassen leeftijd. Wel staan hersentumoren dan op de 2e plek qua voorkomen bij kinderen die de diagnose kanker krijgen.

Het woord hersentumor is een verzamelnaam en omvat zeer veel verschillende type tumoren met hun eigen kenmerken, eigen gedrag en eigen manier van behandeling.

Hersentumoren worden genoemd naar het type hersencel waar zij uit ontstaan zijn. Een hersentumor die ontstaat uit cellen die in hersenvliezen (meningen) zitten wordt een meningeoom genoemd. Een hersentumor die ontstaat uit gliacellen (ondersteunende cellen in de hersenen) een glioom.

De gliomen worden nog weer verder onder verdeeld. Er bestaan namelijk 3 verschillende type gliacellen namelijk atsrocyten, oligodendrocyten en ependymcellen. Deze kunnen elk zorgen voor het ontstaan van een specifiek type tumor.

De WHO heeft alle tumoren onderverdeeld in 4 groepen, genummerd van 1 t/m 4. Graad I tumoren zijn de minst kwaadaardig type hersentumoren. Sommige mensen willen deze groep ook wel goedaardig noemen. Graad IV tumpren zijn de meest kwaadaardig type tumoren. De WHO-indeling kijkt naar de celmorfologie (in hoeverre is het oorspronkelijk celtype nog herkenbaar), hoeveel heid cellen, de mate van celdeling, toename van bloedvaatjes in de tumor (neovascularisatie) en de mate waarin er dood weefsel aanwezig is in de tumor (necrose).
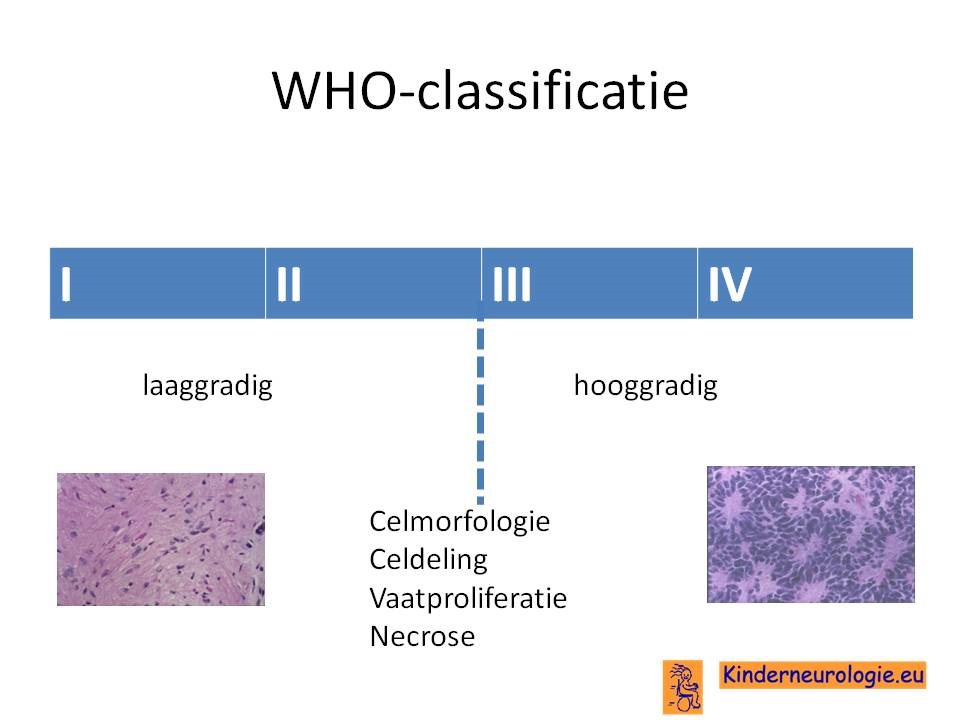
Op deze manier kan een veelvoorkomend type glioom: het astrocytoom nog weer verder onder verdeeld worden in subtypes. Een pilocytair astrocytoom (WHO graad 1) gedraagt zich heel anders dan een glioblastoom (WHO graad 4) ook al zijn het tumoren uit dezelfde subgroep. WHO graad 1 en 2 tumoren worden ook wel laaggradige gliomen genoemd en WHO graad 3 en 4 tumoren hooggradige gliomen.
Bepaald type hersentumoren hebben vaker (maar niet altijd) een lage of een hoge WHO-graad.

Genetisch onderzoek gaat ook een steeds belangrijkere rol spelen bij het stellen van de juiste diagnose. Bepaalde mutaties komen alleen bij een bepaald type tumor voor.
Vroeger werd de term oligo-astrocytoom wel gebruikt wanneer niet duidelijk was of er sprake was van een oligodendroglioom of een astrocytoom. Met behulp van moleculaire genetica kan nu beter onderscheid gemaakt worden, wanneer er sprake is van een 1p/19q deletie wordt er gesproken van een oligodendroglioom.

Symptomen van een hersentumoren
De plaats van de hersentumor bepaalt de symptomen die veroorzaakt worden door de hersentumor. Grofweg zijn deze symptomen in 3 groepen onder te verdelen:

De plaats van de tumor bepaalt welke focale uitvalsverschijnselen kunnen ontstaan

Wanneer tumoren veel ruimte innemen of wanneer een hydrocefalus ontstaat als gevolg van de tumor kunnen symptomen ontstaan die wijzen op verhoogde intracraniele druk.

Diagnostiek hersentumoren
De basisdiagnostiek voor het vast stellen van een hersentumor is een MRI scan met contrastvloeistof. Een CT-scan is niet voldoende, net als een MRI scan zonder contrastvloeistof.
Bij hooggradige tumoren zal ook een MRI van het myelum gemaakt worden om te kijken of er aanwijzingen zijn voor uitzaaiingen, bij laaggradige tumoren is dit vaak niet nodig.
Voor de definitieve diagnose is meestal pathologische onderzoek nodig. Weefsel voor PA kan verkregen worden door middel van een biopt of verkregen worden tijdens tumorresectie door de neurochirurg. Nadeel aan een biopt is dat er risico bestaat op een sample error waardoor de WHO graad te laag wordt ingeschat.

Qua behandeling zijn er verschillende mogelijkheden. Dexamethason kan ingezet worden om oedeem rondom de tumor te verminderen. De beste behandeling voor een persoon wordt bepaald in een multidisciplinair overleg en in shared-decision making met de persoon die een hersentumor heeft.

Dexamethason kan in het acute stadium worden ingezet om snel klachten te verminderen. Het vermindert oedeem rondom de tumor en daarmee afname van symptomen. Dexamethason heeft ook nadelen, zoals een verhoogd risico op hyperglycaemie (zeker bij mensen met diabetes), vochtretentie en gedragsveranderingen. Per persoon moeten mogelijke voor- en nadelen afgewogen worden.
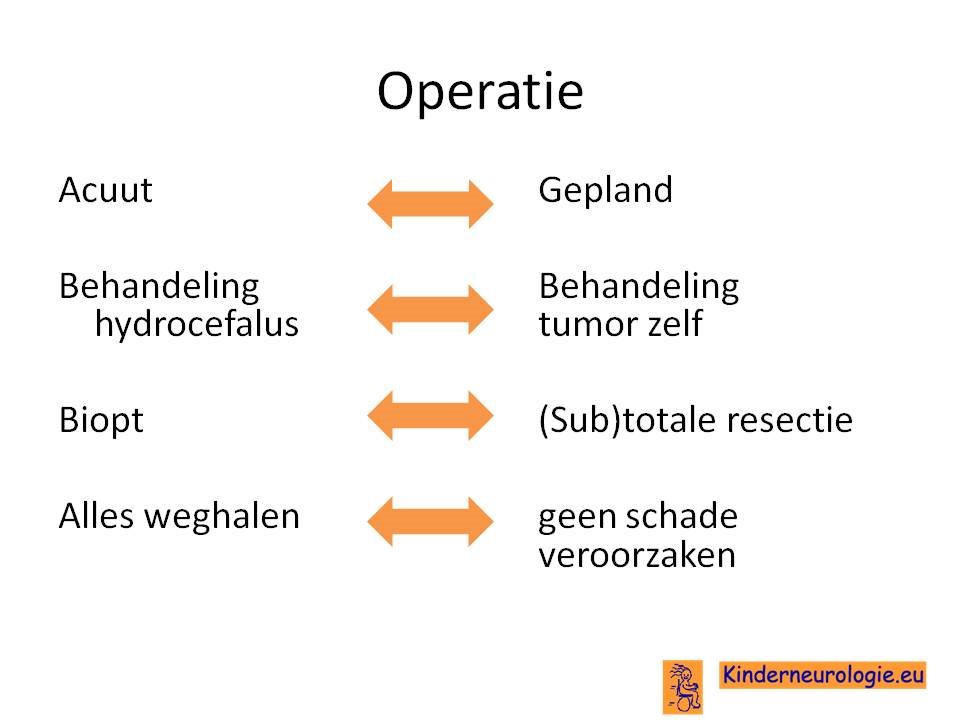
 Voor de meeste hersentumor bestaat de behandeling uit een operatie door de neurochirurg. Er bestaan verschillende type operaties die afhankelijk zijn van de mate van urgentie waarmee geopereerd moet worden en het doel dat met de operatie bereikt moet worden. Tegenwoordig bestaan er steeds meer mogelijkheden voor operatieve monitoring tijdens de operatie om zo schade als gevolg van de operatie zo veel mogelijk te voorkomen. Ook wordt er gebruik gemaakt van fluoresecentietechnieken om goed te kunnen zien welk weefsel allemaal verwijderd moet worden.
Voor de meeste hersentumor bestaat de behandeling uit een operatie door de neurochirurg. Er bestaan verschillende type operaties die afhankelijk zijn van de mate van urgentie waarmee geopereerd moet worden en het doel dat met de operatie bereikt moet worden. Tegenwoordig bestaan er steeds meer mogelijkheden voor operatieve monitoring tijdens de operatie om zo schade als gevolg van de operatie zo veel mogelijk te voorkomen. Ook wordt er gebruik gemaakt van fluoresecentietechnieken om goed te kunnen zien welk weefsel allemaal verwijderd moet worden.
Bepaalde hersentumoren reageren goed op bestraling. Er bestaan verschillende soorten bestraling zoals focale bestraling en gehele schedelbestraling, er kan gekozen worden uit fotonentherapie of protonentherapie. Ook kunnen kleine tumoren behandeld worden met stereotactische bestraling.

Bestraling maakt gebruik van hoogenergetische straling die ionisaties veroorzaakt waardoor radicalen ontstaan. Deze radicalen geven schade aan het DNA van een cel. DNA schade boven een bepaalde drempelwaarde leidt tot celdood. Deze drempelwaarde ligt in tumorcellen lager dan in gezonde hersencellen, gezonde hersencellen hebben meer DNA herstelcapaciteit. Door de bestraling in fracties aan te bieden, krijgen de gezonde hersencellen de tijd om DNA schade te herstellen. De duur van de bestraling varieert meestal tussen de 1 en 7 weken.
Bepaalde hersentumoren reageren goed op chemotherapie. Chemotherapie wordt vooral bij hooggradige gliomen ingezet.

De genetica gaat ook een steeds grotere rol spelen bij de therapie keuze. Bepaalde veranderingen in het DNA maken dat de tumor gevoeliger is voor het geven van chemotherapie. Een 1p/19q deletie wijst op de diagnose oligodendroglioom die goed reageren op PCV-chemotherapie (procabazine, lomustine en vincristine), een MGMT-methyleringsprofiel voorspelt een goed effect van temozolamide.

Het type tumor en/of de conditie van de persoon die de hersentumor heeft kunnen maken dat er geen plaats meer is voor tumorgerichte behandeling. Er wordt dan gekozen voor best supportive care.
De Karnofsky performance scale wordt gebruikt als maat voor de conditie van de persoon met een hersentumor en speelt een belangrijke rol bij het bepalen welke behandeling het best passend is.

Het achteruitgang op de Karnofsky performance scale kan maken dat de nadruk in de behandeling verschuift van tumorgerichte behandeling naar symptoomgerichte behandeling.

Het Landelijk Werkverband Neuro Oncologie (LWNO) heeft op de website www.lwno.nl twee informatiebrieven staan voor personen met een hersentumor, hun naasten en de huisarts met adviezen voor de laatste levensfase.
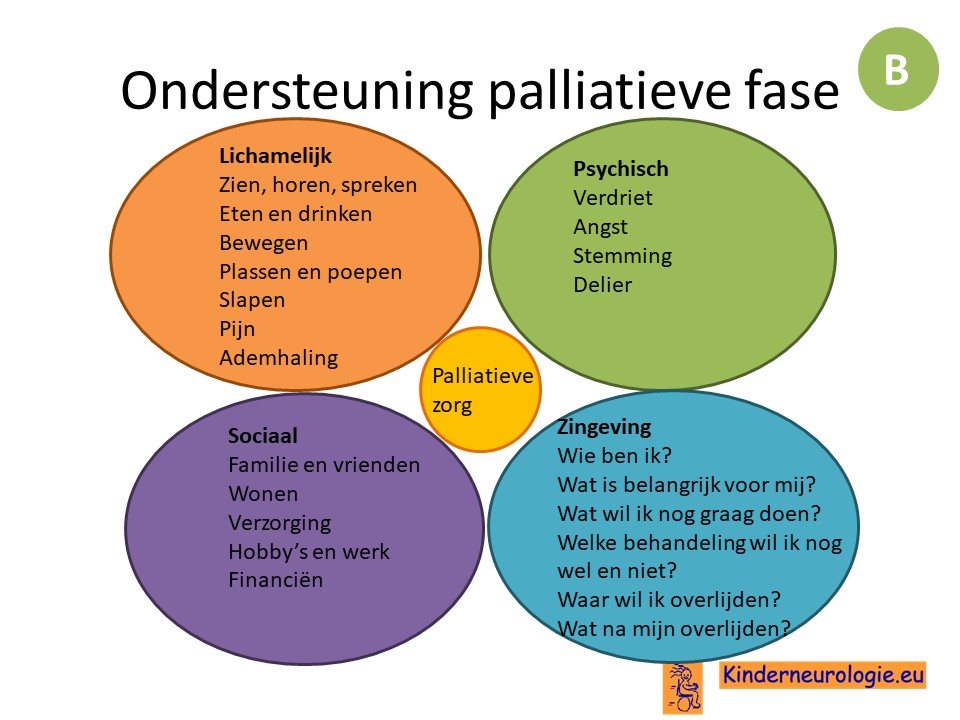
Binnen de palliatieve zorg is het belangrijk om op de vier verschillende domeinen (lichamelijk, psychisch, sociaal en zingeving) te kijken wat belangrijk is voor de persoon met een hersentumor en een plan op maat te maken.
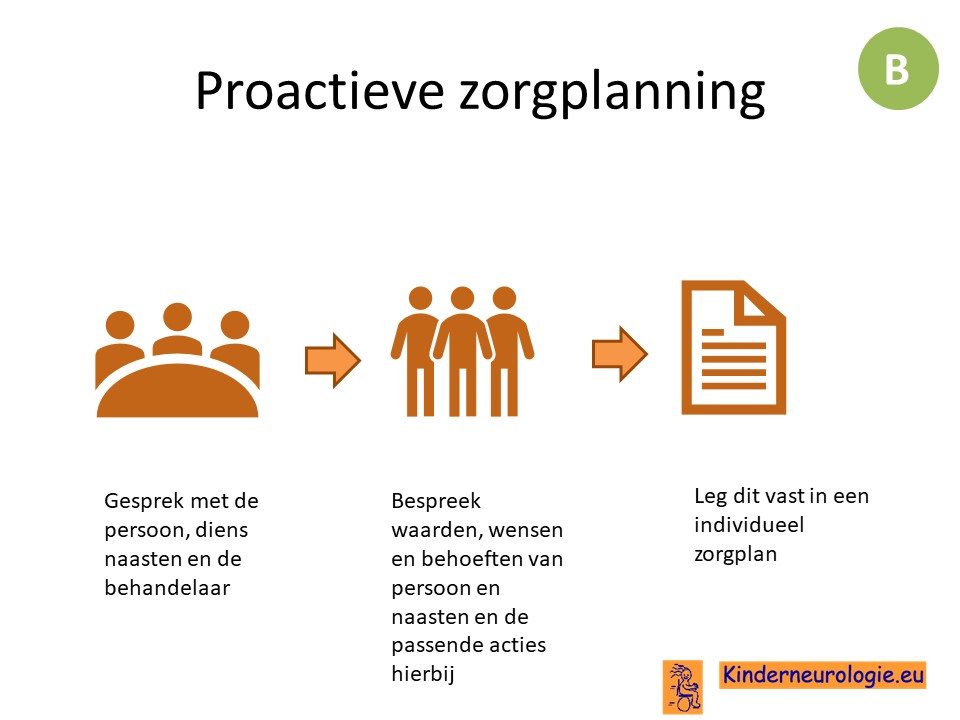
Het is belangrijk om ook vooruit te denken welke symptomen mogelijk kunnen ontstaan en een plan klaar te hebben hoe in deze situatie te handelen, dit heet pro-actieve zorgplanning.
Laatst bijgewerkt: 15 april 2026
Verschillende typen hersentumoren
Primaire hersentumoren
De meest voorkomende hersentumor is het meningeoom, gevolgd door het glioom.
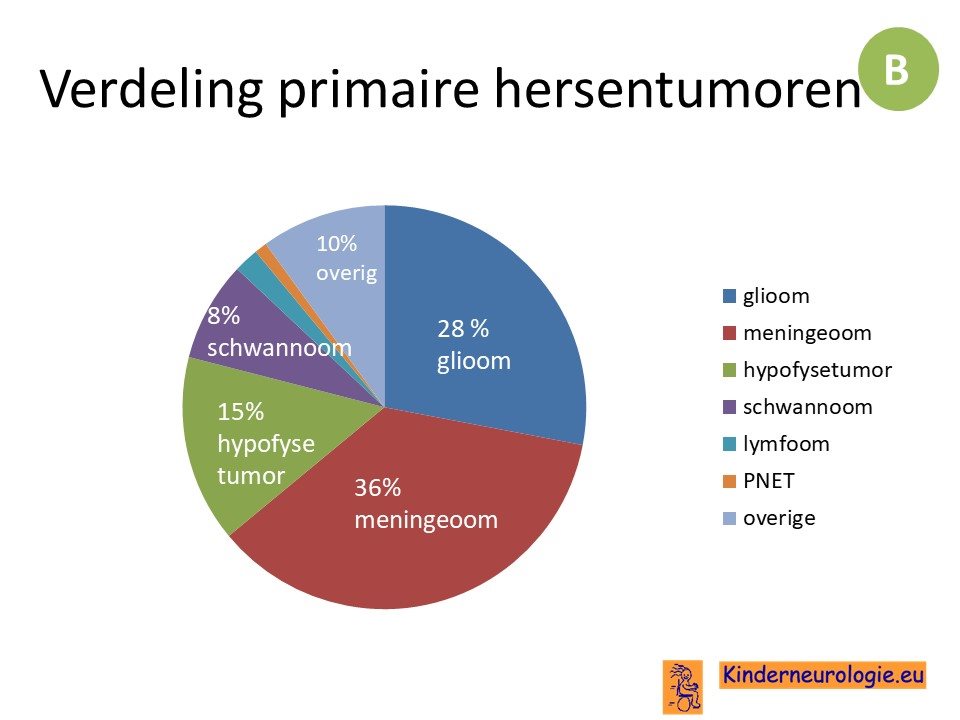
Het meningeoom
Zo'n 40% van alle hersentumoren bij volwassenen is een meningeoom. De mediane leeftijd bij diagnose is 66 jaar. De incidentie van meningeomen neemt de laatste jaren toe, deels vanwege verbeterde beeldvorming en deels ook vanwege toename van het aantal ouderen. Meningeomen komen vaker voor bij vrouwen dan bij mannen.

Bij een klein deel van de mensen is er sprake van 2 of meerdere meningeomen. Dit wordt meningeomatose genoemd. Bij deze mensen is er vaker sprake geweest van schedelbestraling in het verleden of van een onderliggend syndroom waardoor er een vergrote kans bestaat op het krijgen van meningeomen.

Een meningeoom ontstaat uit archnoidale cellen. Door een opeenstapeling van mutaties ontstaat een meningeoom.

Meningeomen worden onder verdeeld in WHO graad 1, graad 2 en graad 3 meningeomen. Meningeoom graad 3 meningeomen worden maligne meningeomen genoemd.
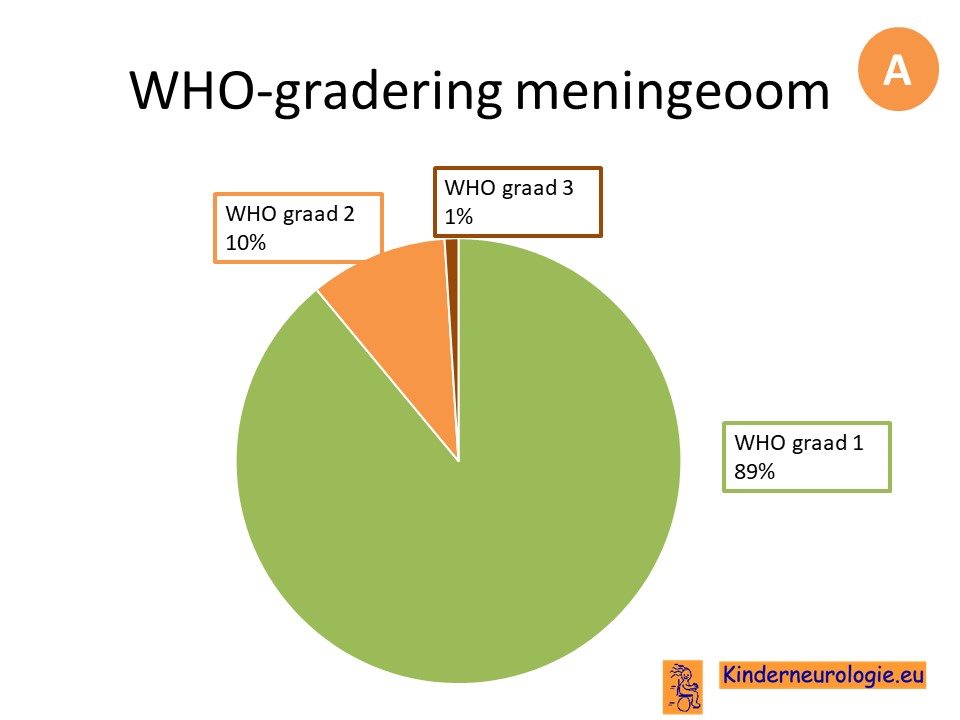
Meningeomen komen het vaakst voor aan de convexiteit, gevolgd door de schedelbasis of de achterste schedelgroeve.
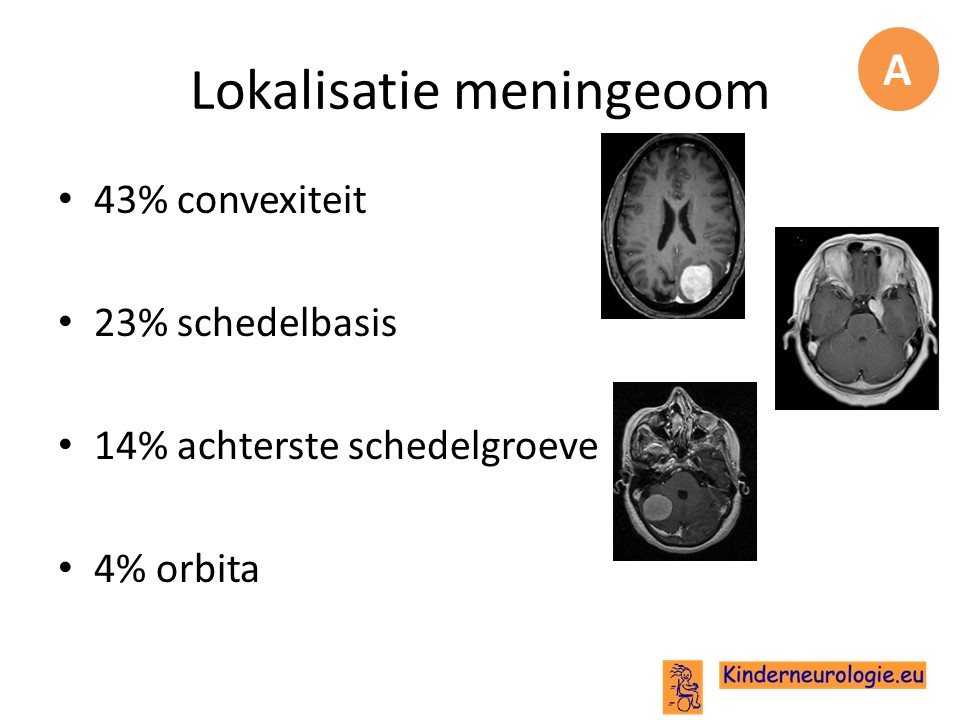
Meningeomen worden vaak per toeval ontdekt wanneer er een scan van het hoofd wordt gemaakt. Dit worden asymptomatische meningeomen genoemd. Wanneer meningeomen klachten geven zijn de meest voorkomende klachten hoofdpijn en epileptische aanvallen.

Een meningeoom heeft specifieke kenmerken op een MRI-scan. Bij deze typische kenmerken kan de diagnose met behulp van de MRI worden gesteld en wordt er geen PA-verkregen. Bij 60% van de mensen met een meningeoom wordt de diagnose alleen met behulp van de MRI-scan gesteld.
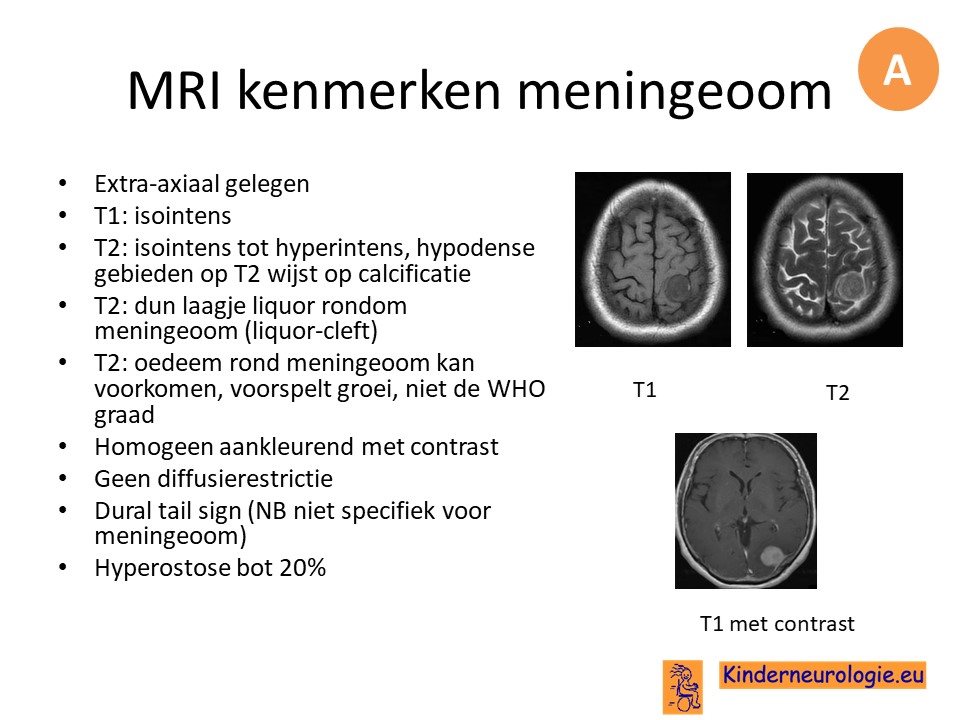
Andere tumoren die een vergelijkbaar beeld kunnen geven als een meningeoom zijn durale metastasen en een lymfoom. Vaak is dan al bekend dat deze mensen een solide of hematologische maligniteit hebben.

Een meningeoom heeft niet altijd een behandeling nodig, zeker niet als er geen symptomen zijn en het meningeoom niet groeit.
Wanneer het meningeoom geen behandeling nodig heeft, worden met een bepaalde regelmaat MRI-scans gemaakt om het meningeoom te vervolgen.
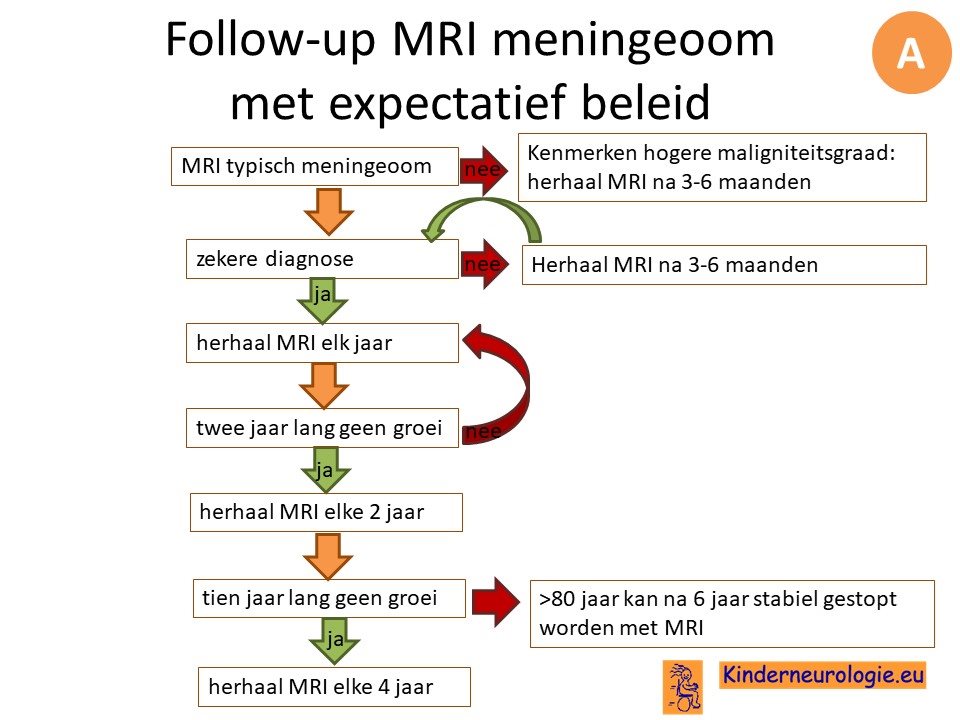
Behandeling wordt overwogen wanneer er sprake is van symptomen, groei of een grote kans op groei in de toekomst. Per patiënt moeten de voor- en nadelen van een mogelijke behandeling worden afgewogen.

Bepaalde kenmerken van de patiënt of van het meningeoom maken de kans op groei groter.

De eerste keus behandeling van een meningeoom is een operatie waarbij het doel is de tumor in zijn geheel te verwijderen, inclusief het aankleurende deel van de dura op de MRI-scan. Bij WHO graad 3 tumoren is aanvullende radiotherapie nodig, bij WHO graad 2 tumoren met een rest kan dit ook overwogen worden.

De prognose van een meningeoom hangt af van de WHO-gradering. Omdat een meningeoom vaker bij mensen met oudere leeftijd voorkomt, is de reden van overlijden ook vaak een andere dan het meningeoom zelf.

Kans op recidief
Bij het bepalen van de kans op recidief van een meningeoom wordt aan de ene kant gekeken naar DNA kenmerken van het meningoom (tumorprofiel), en aan de andere kant door het aantal immuuncellen in de tumor te bepalen (tumor-micro-omgeving)
Gliomen
Na meningeomen, zijn gliomen de meest voorkomende primaire hersentumor.
Gliomen zijn tumoren die ontstaat uit gliacellen. In deze gliacellen ontstaan meerdere mutaties in het DNA waardoor uit de gliacel een tumor ontstaat.
Gliomen werden vroeger ingedeeld aan de hand van kenmerken bij PA-onderzoek (histopathologische indeling)

In gliomen worden verschillende mutaties in het DNA gevonden, deze mutaties kunnen een classificerend zijn en soms ook het effect van behandeling voorspellen.

In 2021 is er een nieuwe WHO-indeling gemaakt voor gliomen, waarbij histopathologische naam worden gecombineerd met de moleculaire genetica van de tumor en de WHO graad.
75% van alle gliomen is een glioblastoom graad 4.

Aan de hand van moleculaire genetica in een glioom, wordt het type glioom bepaald.
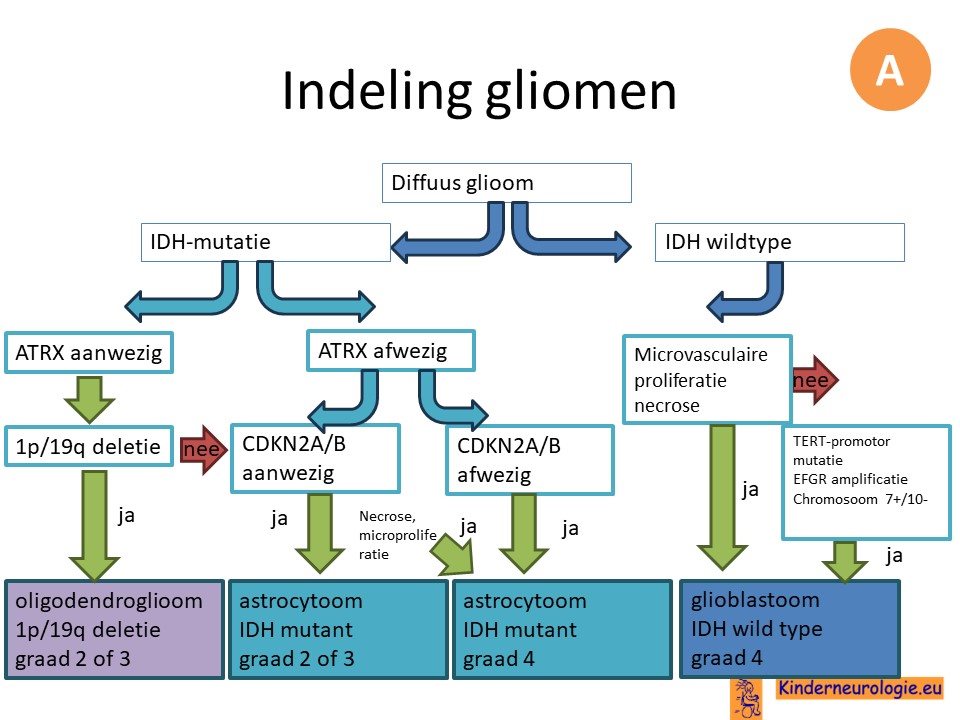
Belangrijk is in deze nieuwe indeling dat een astrocytoom graad 4 IDH mutant een ander type is dan het glioblastoom IDH wildtype.
De term glioblastoma multiforme wordt tegenwoordig niet meer gebruikt.
Daarnaast bestaan er WHO graad 1 tumoren, die vaak op de kinderleeftijd en bij jong volwassenen worden gezien. Zij zijn niet diffuus groeiend en hebben een veel betere prognose, deze tumoren worden zelden hooggradig.


Voor de diagnostiek van een glioom is de combinatie van MRI bevindingen met weefseldiagnostiek inclusief moleculair genetische technieken nodig.

De behandeling van gliomen bestaat uit een zo volledige mogelijke verwijdering door operatie (maximaal veilige resectie vaak in combinatie met radiotherapie en chemotherapie. Bij graad 2 tumoren worden radiotherapie en chemotherapie alleen gegeven wanneer er kenmerken zijn van hoog risico op snelle progressie. Het beste behandelbeleid wordt bepaald tijdens een multidisciplinair overleg. De leeftijd van de persoon en de mate van functioneren (Karnofsky performance scale) bepalen mede de best passende behandeling.

Immuun checkpoint inhibitors hebben bij gliomen geen overlevingsvoordeel.
Bij recidief tumorgroei na behandeling zijn er geen standaard behandelopties en zal in een MDO gekeken per persoon gekeken moeten worden wat de beste behandeloptie is. Vaak is dat best supportive care zonder specifiek op de tumor gericht behandeling. Bij het glioblastoom kan een behandeling met lomustine (CCNU) worden overwogen wanneer de persoon nog in goede conditie is. Deze tweede lijns behandelingen worden vaak in studieverband gegeven.
De prognose van het glioom hangt sterk samen met de leeftijd van de persoon op moment diagnose, van het functioneren van de persoon van de WHO-graad van de tumor en van de moleculaire genetische bevindingen.
Oligodendrogliomen graad 2 hebben bij volwassenen de beste prognose van de diffuse gliomen en glioblastoom graad 4 heeft de slechtste prognose.

Ander type tumoren
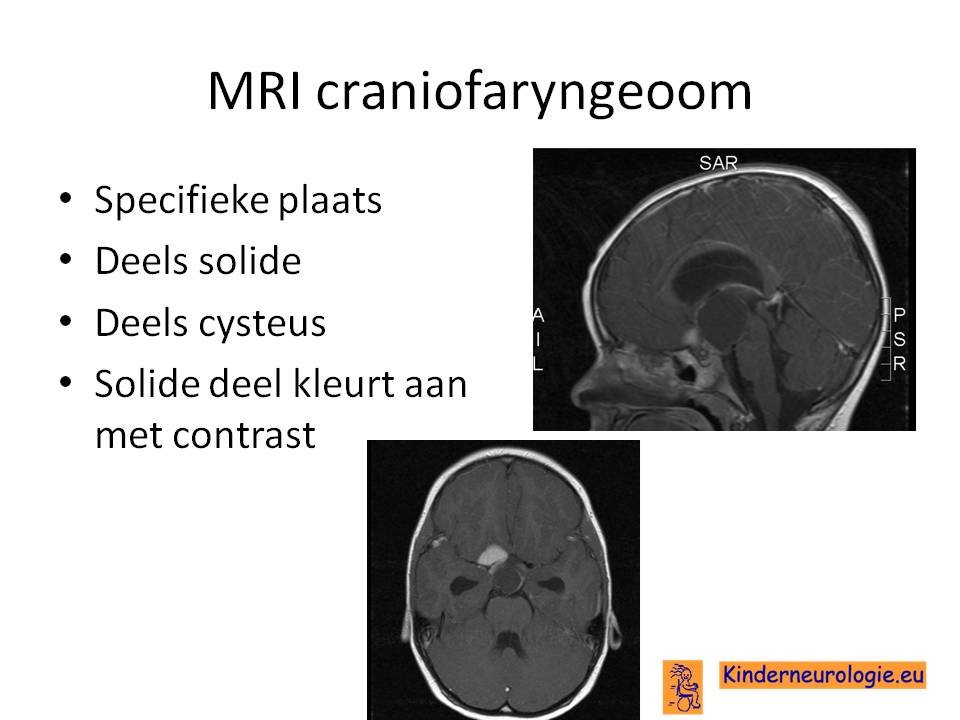
- Craniofaryngeoom

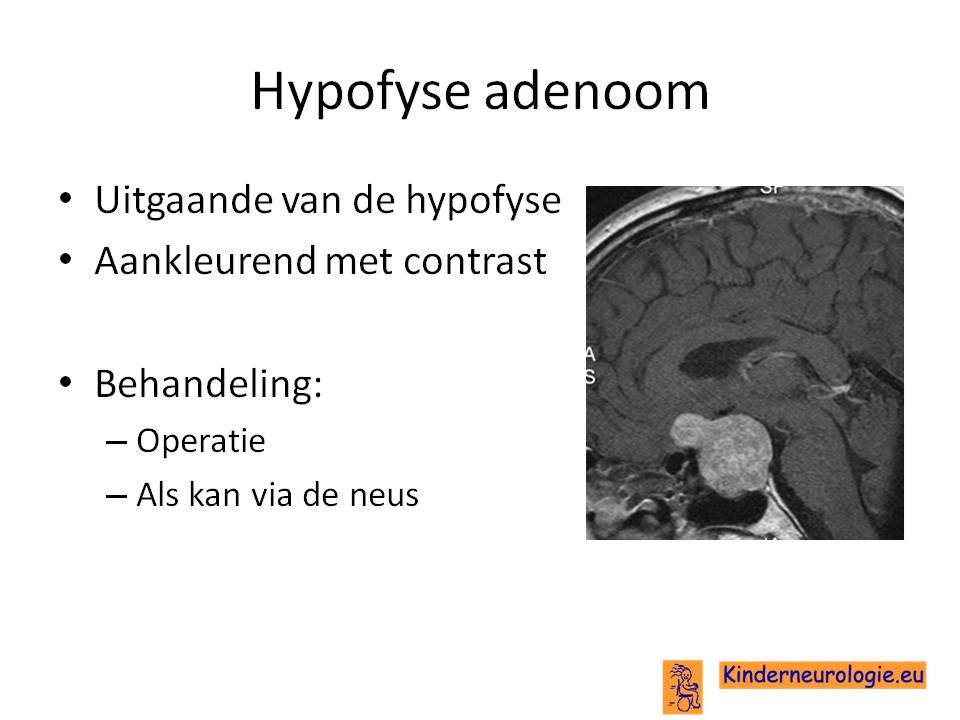
- Hypofyse adenoom
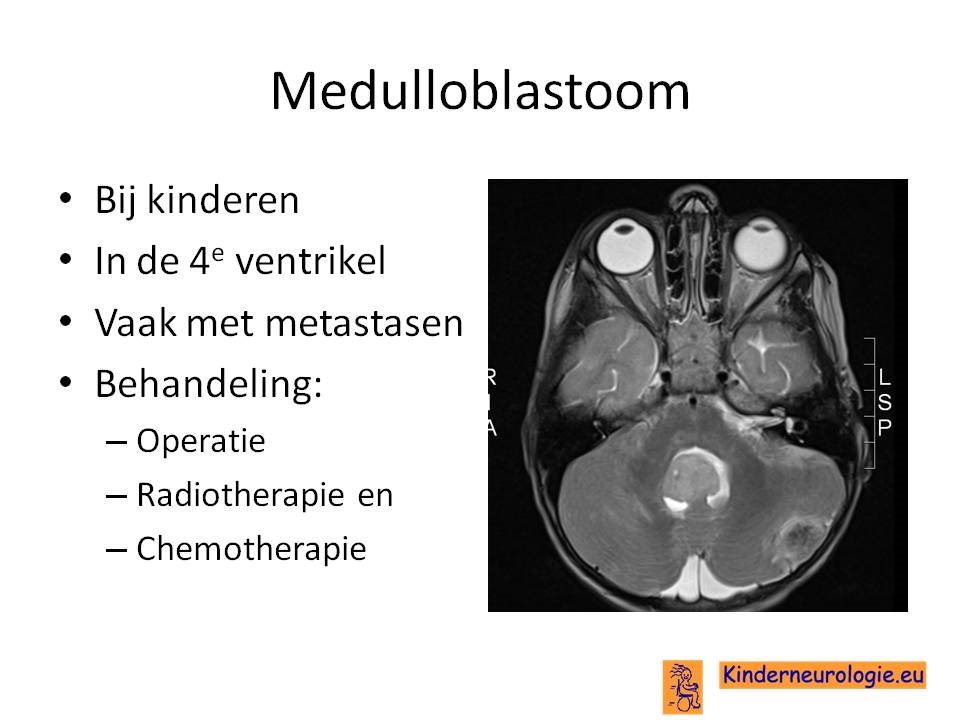
- Medulloblastoom
De prognose van een hersentumor hangt sterk samen met het type tumor. Ook per type tumor is er een groot verschil in prognose voor de individuele patient.
Er komt steeds meer kennis dat het wel of niet hebben van een bepaalde mutaties in een tumor van invloed is op de prognose. Inmiddels is dit van een paar mutaties bekend.

laatst bijgewerkt: 15 april 2026
Ruggenmergtumoren


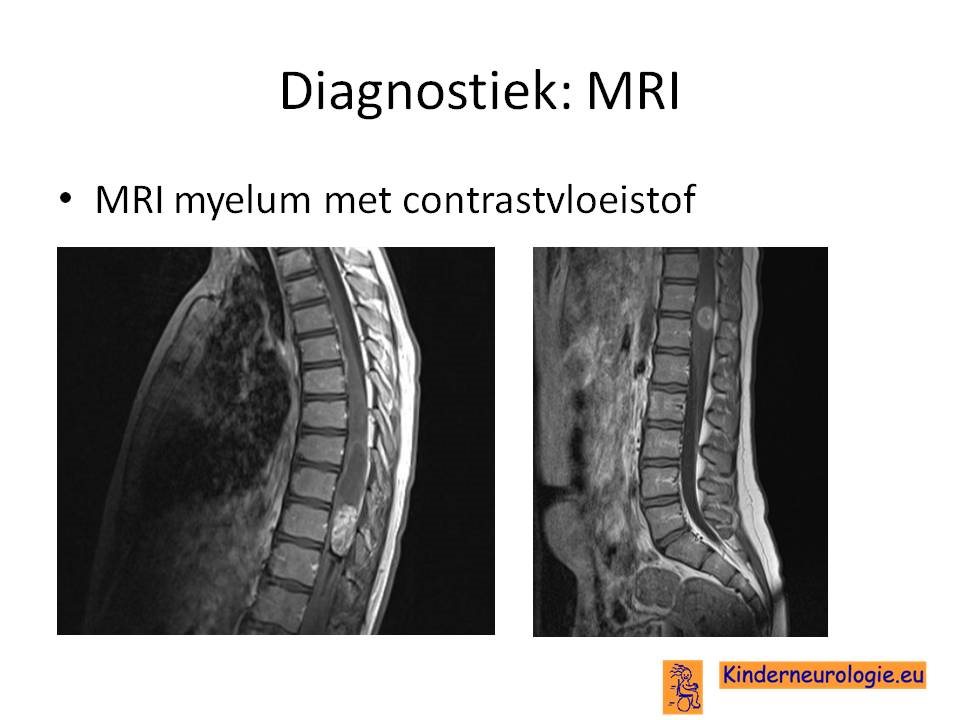
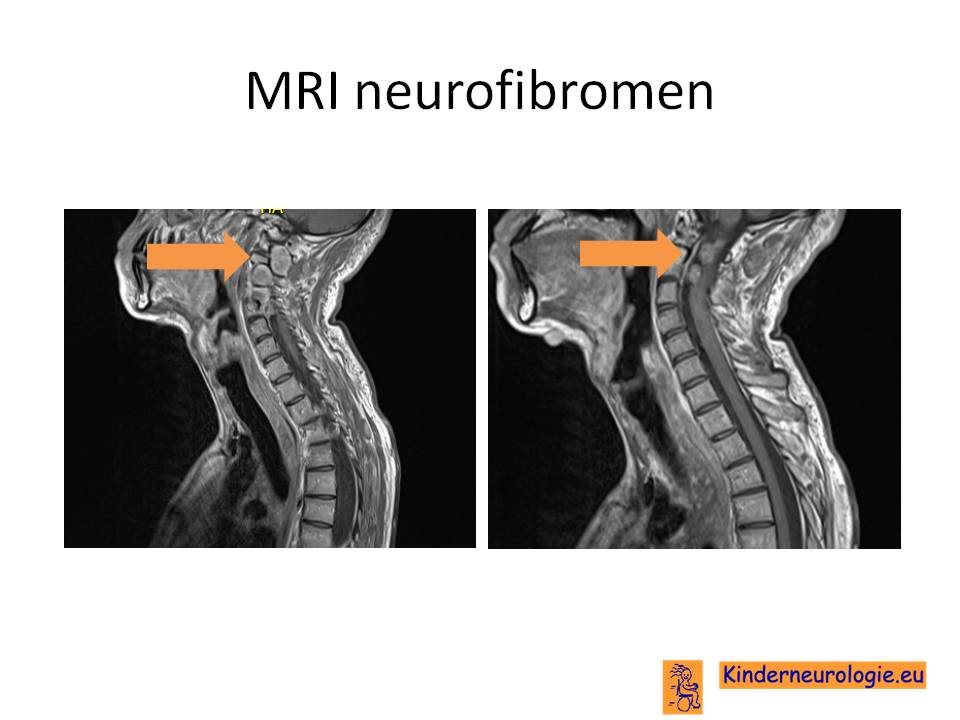

Metastasen
Metastasen
Een tumor elders in het lichaam (meestal een carcinoom) kan zorgen voor uitzaaiingen naar het zenuwstelsel toe. Deze uitzaaiingen worden metastasen genoemd. Metastasen worden meestal gezien in de hersenen, de hersenvliezen of in de wervels en de epidurale ruimte.

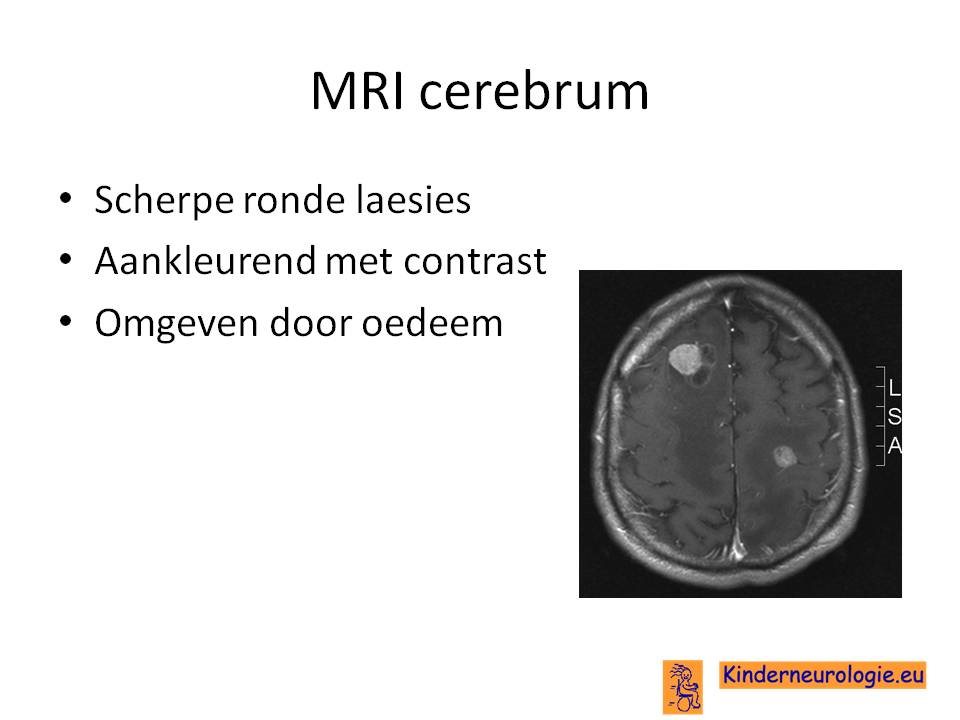
Hersenmetastasen
Hersenmetastasen
Hersenmetastasen komen regelmatig voor.

De meest voorkomende primaire tumoren die hersenmetastasen geven zijn long en mammacarcinoom.



Het doel van de behandeling van hersenmetastasen is palliatief met als belangrijkste doel een zo goed mogelijk behoud van functioneren. Het beleid kan het beste worden bepaald in een multidisciplinair overleg (MDO). De beste beleidskeuze hangt af van de klinische conditie van de persoon, de aanwezigheid van systemische metastasen naast hersenmetastasen en systemische behandelopties.

Naast chemotherapie kan tegenwoordig immuuntherapie ook een behandeloptie zijn. Deze behandeling is inmiddels voor meer dan 50 verschillende tumoren mogelijk waaronder het melanoom, niet kleincellig longcarcinoom, colorectaal carcinoom, niercelcarcinoom en uortheelcelcarcinoom.
Er bestaan verschillende vormen van immuuntherapie.

De middelen verschillen in de kans op respons en de snelheid waarmee de respons optreedt en de duur van de respons, de groeisnelheid van de hersenmetastasen is daarom een belangrijke factor welke behandeling nodig is. Dexamethason verlaagt de respons kans van immuuncheckpoint inhibitors, daarom moet de dosering dexamethason lager zijn dan 3 mg per dag en het liefst lager dan 1,5 mg per dag.

De prognose van hersenmetastasen is somber, bij respons op immuuntherapie kan bij een deel van de mensen een langerdurende ziektecontrole worden bereikt.

laatst bijgewerkt: 15 april 2026
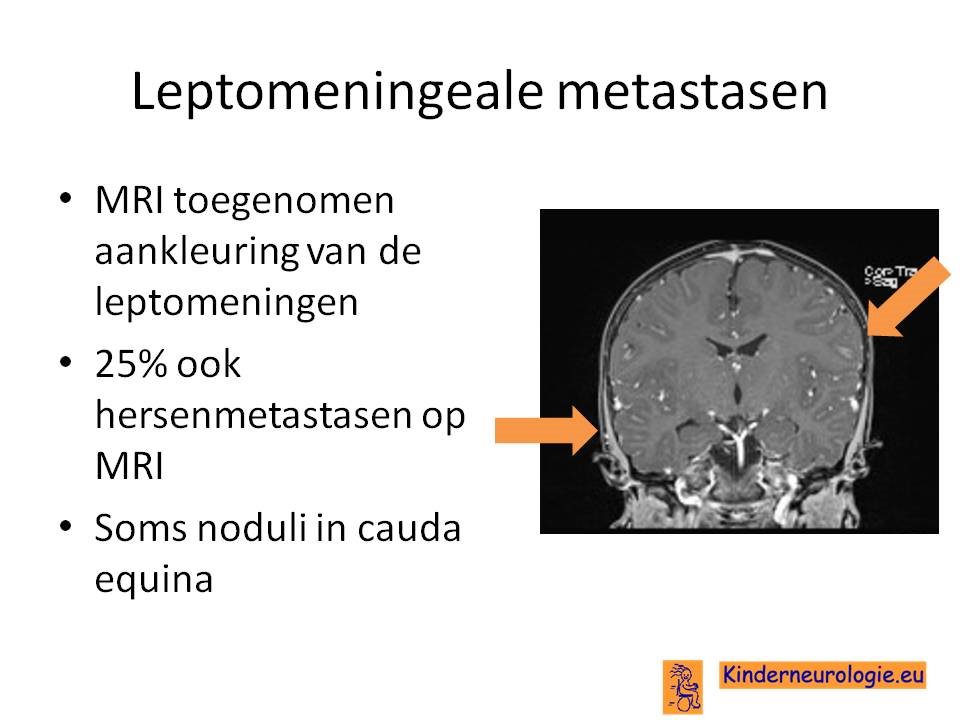
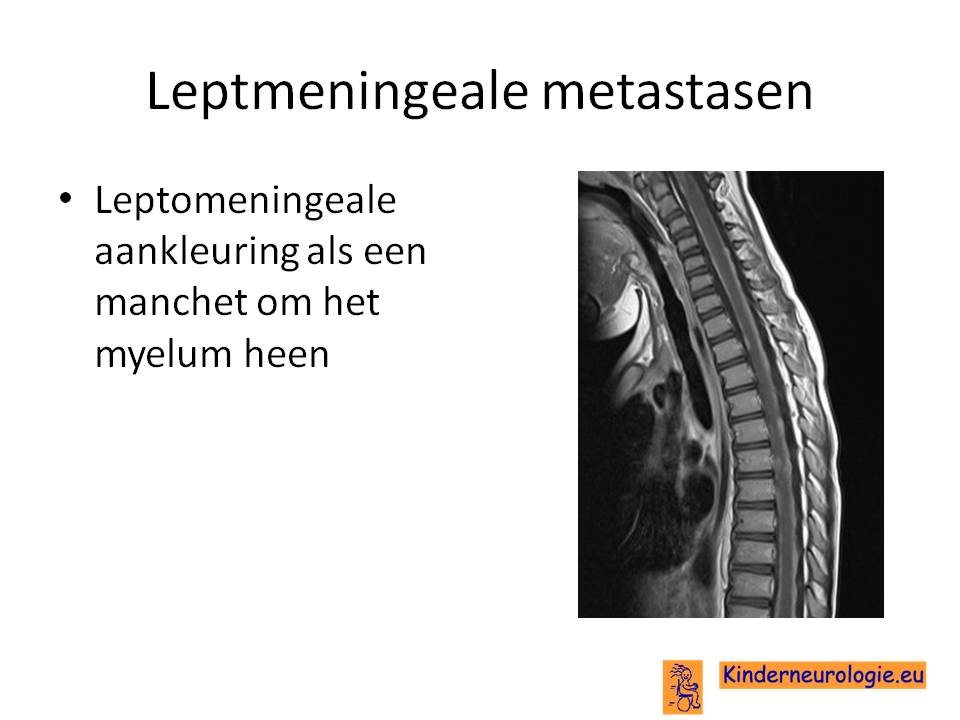
Leptomeningeale metastasen





Metastasen naar epidurale ruimte
Epidurale metastasen ontstaan meestal door doorgroei van wervelmetastsen naar de epidurale ruimte. Wervelmetastasen komen vaak voor in een laat stadium bij patienten met een carcinoom, een klein deel hiervan krijgt epidurale metastsen. Meestal zitten deze in de thoracale wervelkolom.

Epidurale metastasen kunnen bij veel verschillende tumoren zowel carcinomen als hematologische malginiteiten voorkomen.

Het meestvoorkomende symptoom is pijn, lokaal of radiculair. Door compressie van de epidurale ruimte kan een partiele dwarslaesie of een cauda syndroom ontstaan.

De diagnostiek bestaat uit een MRI van de gehele wervelkolom. Metastasen komen namelijk bij 30% van de patienten op meerdere plekken voor zonder onderlinge verbinding.
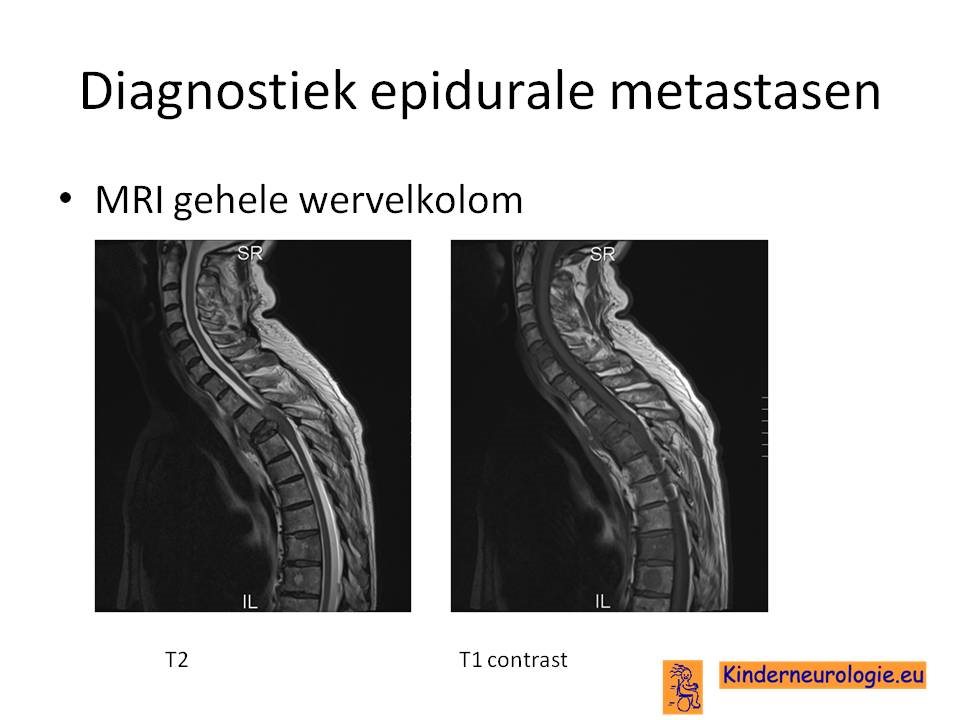
Bij iedere patient met een tumor in de recente voorgeschiedenis en een van onderstaande symptomen moet een MRI gemaakt worden op korte termijn.

Paraneoplatische syndromen

Er bestaan veel verschillende type paraneoplastische syndromen.

Paraneoplastische syndroom komen bij bepaalde type tumoren vaker voor, maar kunnen in principe bij ieder type tumor, behalve de primare hersentumoren voorkomen. Bij elk type tumor kan in principe ook elk type paraneoplastisch syndroom voorkomen. Bepaalde type paraneoplastische syndromen komen wel vaker voor bij bepaald type tumoren zoals een anti-NMDA receptor encefalits bij een gynaecologische tumor, een sensore neuronopathie bij klein cellig longcarcinoom en een opsoclonus myoclonus syndroom bij een neuroblastoom.

De diagnose wordt gesteld op grond van het klinische beeld. Omdat de primaire tumor vaak nog niet bekend is, moet gezocht worden naar de primaire tumor. Liquor onderzoek toont vaak een licht verhoogd celgetal en een licht verhoogd eiwitgehalte. Auto-antistoffen kunnen bij een deel van de patienten worden aangetoond.

Met behulp van immunosupressiva wordt geprobeerd de auto-immuunreactie te onderdrukken. Dit is vaak moeilijk, meerdere immunosupressiva moeten worden toegepast.
Voor bepaalde paraneoplastische syndromen bestaat een specifieke symptoom behandeling.

Het paraneoplastisch beeld blijft vaak bestaan ondanks de behandeling. Behandeling is dan met name bedoeld om verergering van het klinische beeld tegen te gaan.
Patienten met een paraneoplastisch syndroom hebben qua tumor meestal een betere prognose dan patienten zonder paraneoplastisch syndroom.

Bijwerkingen behandeling tumor
Behandelingen kennen ook altijd bijwerkingen. Het is belangrijk om deze bijwerkingen te kennen, zodat deze meegenomen kunnen worden in de afweging welke behandeling het beste passend is. Daarnaast is het goed in kader van pro-actieve zorgplanning een plan te hebben hoe op deze bijwerkingen te reageren.
Een vaak ingezette behandeling bij tumoren is radiotherapie. Radiotherapie kan zowel op de korte als de lange termijn bijwerkingen hebben. De korte termijn bijwerkingen zijn vaak aanwezig tijdens de bestraling en verdwijnen weer binnen 3 maanden na einde van de bestraling. Bij veel bijwerkingen kunnen de bijwerkingen verminderd worden door het medicijn dexamethason.

Lange termijn bijwerkingen ontstaan na maanden of jaren en zijn meestal blijvende bijwerkingen.

Een ander veel ingezette behandeling is chemotherapie. Nadeel aan chemotherapie is dat niet alle chemotherapie vanwege de bloedhersenbarriere goed in het centraal zenuwstelsel terecht komt om daar zijn werk te kunnen doen.

Binnen de behandeling van systemische tumoren wordt steeds vaker immuuntherapie ingezet.
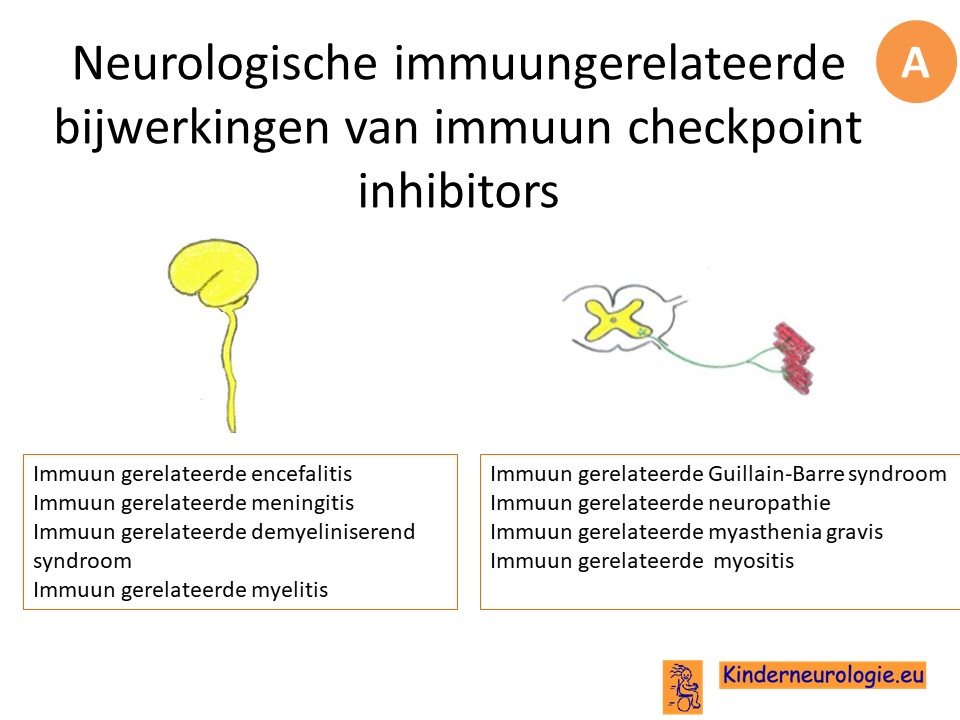
Een van deze vormen van immuuntherapie zijn zogenaamde immune checkpoint inhibitors (ICI). Deze behandelingen gaan het onderdrukkende effect van de tumor op het immuunsysteem tegen.
Deze behandelingen kunnen neurologische bijwerkingen geven, neurologische Immuungerelateerde bijwerkingen genoemd (nIRAE). Deze komen bij 1-12% van de behandelde mensen met ICI voor. Het gaat meestal om immuungerelateerde bijwerkingen van het centrale of van het perifere zenuwstelsel.
Deze bijwerkingen kunnen reden zijn voor staken van de immuuntherapie.
De gradering van de impact van de bijwerkingen bepaalt het te volgen beleid.

Bij milde symptomen die niet van invloed zijn op het dagelijks functioneren kan afgewacht worden en het klinisch beeld vervolgd worden. Bij symptomen die meer impact hebben, wordt de ICI behandeling gestaakt (tijdelijk of permanent) en een behandeling met prednison gegeven. De dosering hangt af van de ernst van de klachten. Dit wordt 4-8 weken gegeven en daarna wordt geprobeerd de dosering prednison weer af te bouwen. Bij ernstige klachten of onvoldoende effect van prednison kunnen immuunglobulines en/of plasmaferese worden toegevoegd.

Verklaring van de kleuren en bolletjes op de afbeeldingen. Deze geven voor geneeskunde studenten en arts-assistenten over welke kennis zij zouden moeten beschikken.

Meer informatie
Auteur: JH Schieving
Referenties
- Biemond cursus neuro-oncologie 2014 en 2024
Laatst bijgewerkt: 29 december 2024 en 15 december 2014
